|
Трихомониаз - заболевание
мочеполовой системы, вызываемое простейшим одноклеточным паразитом
Trichomonas vaginalis. Заболевание передаётся половым путём
и, в крайне редких случаях, возможно заражение через
контаминированные (зараженные) поверхности. В мире трихомониазом
страдает примерно 170 млн. человек. Болезнь не имеет сезонного
характера, поражает все слои населения. Несмотря на интенсивное
изучение, имеются определённые трудности в диагностике трихомониаза
и его лечении.
Этиология
и патогенез.
Инфекционным
агентом трихомониаза человека (синонимы – трихомоноз, трихомонадоз,
трихомониаз) является исключительно Trichomonas vaginalis. По
систематике одноклеточное простейшее Trichomonas vaginalis
относится к царству высших процистов - Protozoa, классу
жгутиковых - Flagella, семейству - Trichomonadidae,
роду - Trichomonas. Человек может быть носителем трёх видов
трихомонад: Trichomonas tenax (elongata), Trichomonas
hominis (abdominalis), Trichomonas vaginalis. В ротовой
полости на кариозных зубах обитает Trichomonas tenax. При
диспепсических расстройствах, обычно у детей и реже у взрослых,
выделяют комменсал толстого кишечника - Trichomonas hominis.
Трихомонадой, живущей в урогенитальном тракте, считается
исключительно Trichomonas vaginalis. Другие человеческие
трихомонады, наблюдаемые при лабораторной диагностике, следует
рассматривать как контаминацию во время забора материала. Такие
ошибки в диагностике трихомониаза чаще случаются при обследовании
детей.
Частота инфицирования трихомониазом
клинически здоровых женщин в развитых странах составляет 2-10% и в
развивающихся 15-40%. Причём в США ежегодно регистрируют примерно 3
млн. новых случаев заболевания женщин (это приблизительно 2,4%. В
России в 1996 году на 100 тыс. населения зарегистрировано 339
(0.34%) случаев заболевания трихомониазом. Данные статистики
указывают на то, что до 40% женщин, посещающих учреждения
дерматовенерологического профиля, являются носителями T.
vaginalis. Зарубежные данные обследования проституток
демонстрируют носительство T. vaginalis до 70%. Возбудитель
заболевания крайне редко обнаруживается у женщин в
постменопаузальном периоде и у девственниц.
Передача Trichomonas vaginalis не половым путём встречается
крайне редко в следующих случаях: использование
высококонтаминированных (обсемененных) дужки душа (биде), сиденья
унитаза и полотенца. Возможность инфицирования женщин паразитом при
купании в естественных водоёмах, бассейне и бане при соблюдении
правил личной гигиены в настоящее время полностью отвергается
вследствие крайне низкой его концентрации в анализируемых образцах
воды. Жизнеспособные Trichomonas vaginalis обнаруживаются в
моче, сперме и необеззараженной воде спустя несколько часов после
выхода из половых путей инфицированного лица, т. к. некоторое время
микроорганизм защищён от высыхания и действия солнечного
ультрафиолета.
 |
|
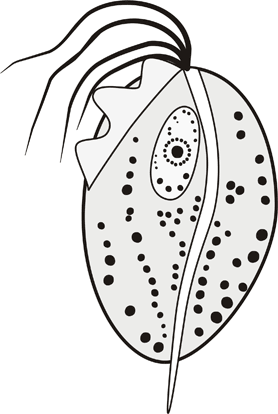
Trichomonas vaginalis
(схема) |
В чистой
культуре Trichomonas vaginalis имеет овальную или округлую
форму длиной 10 мкм и шириной 7 мкм. Внешний вид клетки меняется в
зависимости от физико-химических условий среды и роста. Когда
трихомонада прикрепляется к эпителиальной клетке, она приобретает
амёбовидную форму.
T.vaginalis - это
одноклеточный простейший организм. Он имеет пять жгутиков, четыре из
которых расположены в его передней части, а пятый жгутик (шипик)
располагается внутри ундулирующей (изгибающейся) мембраны,
совершающей волнообразные движения. Жгутики и ундулирующая мембрана
создают паразиту характерные дрожащие движения (при наблюдении в
световой микроскоп движения скорее напоминают дергающиеся, как у
шахматного коня, изредка трихомонада медленно вращается вокруг своей
оси). Причём по длине ундулирующей мембраны при микроскопии можно
отличить T.vaginalis от кишечной трихомонады T.hominis,
которую иногда находят в моче у детей. При неблагоприятных условиях
для роста T.vaginalis трансформируется из амёбовидной формы в
овальную и прячет внутрь свои жгутики. Эти формы несколько
напоминают псевдоцисты, но более вероятно, что они являются
деградационными (дегенеративными) формами возбудителя вследствие
проведенного недавно лечения, т.к. в настоящее время отсутствуют
сведения об их реверсии в активное состояние.
Ядро T.vaginalis расположено в его передней части и окружено
пористой ядерной мембраной. У живых клеток в
световой микроскоп
видны гранулы. Они продуцируют молекулярный водород и были названы
гидрогеносомами (в них происходит обмен веществ паразита,
осуществляется функция "переваривания" веществ).
Существует несколько округлых форм влагалищных трихомонад
наблюдаемых при делении и фазах роста в культуре: без жгутиков, со
жгутиками и делящимся ядром, со жгутиками и множественными ядрами.
Ранее полагали, что эти формы не являются стадиями жизненного цикла,
а скорее возникают при неблагоприятных условиях. Однако, по
последним данным, эти формы могут быть стадиями, предшествующими
появлению одноядерных жгутиковых. Круглые формы морфологически
отличаются от меньших округлых жгутиковых форм.
|
 |
|
Трихомонады на электронной фотографии (Ш –
шипик, Ф – фибриллы [жгутики], УМ –
ундулирующая мембрана) |
|
Т.vaginalis
- это облигатный паразит (не способный длительно существовать вне
организма-хозяина), у которого потеряна способность синтезировать
жизненно необходимые вещества (пурины, пиримидины и многие липиды).
Эти питательные компоненты микроорганизм получает из вагинального
секрета или при фагоцитозе ("поедании") бактериальных клеток
нормальной микрофлоры мочеполовых путей. Для роста трихомонад
особенно важна сыворотка крови, поскольку она содержит липиды,
жирные кислоты, аминокислоты и следы металлов.
In vitro ("в пробирке") T.vaginalis растёт оптимально при рН
(кислотности среды) 6,0 - 6,3 и температуре 35 - 37°С, хотя её рост
осуществляется и в более широком диапазоне рН, особенно в
изменяющейся среде влагалища.
T.vaginalis - это
облигатный паразит (не способный длительно существовать вне
организма-хозяина), у которого потеряна способность синтезировать
жизненно необходимые вещества (пурины, пиримидины и многие липиды).
Эти питательные компоненты микроорганизм получает из вагинального
секрета или при фагоцитозе ("поедании") бактериальных клеток
нормальной микрофлоры мочеполовых путей. Для роста трихомонад
особенно важна сыворотка крови, поскольку она содержит липиды,
жирные кислоты, аминокислоты и следы металлов.
In
vitro ("в пробирке") T.vaginalis растёт оптимально при рН
(кислотности среды) 6,0 - 6,3 и температуре 35 - 37°С, хотя её рост
осуществляется и в более широком диапазоне рН, особенно в
изменяющейся среде влагалища.
 |
|
Трихомонада (цветная
микрофотография) |
Слизистая влагалища является бедной питательной средой для паразита.
А так как трихомонада не способна синтезировать некоторые липиды
(жироподобные вещества) то, вероятно, эритроциты (красные кровяные
клетки) могут быть первичным источником жирных кислот, необходимых
паразиту. В дополнение к липидам, железо является важнейшим
продуктом для T.vaginalis и также может потребляться через
лизис (разрушение) эритроцитов.
Клеточные протеазы (белковые
ферменты) T.vaginalis также способны разрушать
иммуноглобулины G и А (защитные белки организма-хозяина),
присутствующие во влагалище.
T.vaginalis с помощью
специального белка, названного
"клеточный разъединяющий фактор", или
КРФ, (большой гликопротеид размером 200 кДа),
проникает в межклеточное пространство, и, разрыхляя ткань,
способствует проникновению туда бактерий и формированию очага
воспаления. Содержание КРФ у паразита коррелирует с выраженностью
симптомов вагинита (воспаления влагалища).
Очищенный КРФ активен при рН 5,0 - 8,5 с оптимумом активности при рН
6,5 и потерей её ниже рН 4,5. Этот факт является интересным с
клинической точки зрения, поскольку при минимальной разнице значений
рН в норме и при трихомониазе (0,5) начинается активная колонизация
влагалища трихомонадами. Повышение влагалищного рН при трихомониазе
может стать критическим в патогенезе заболевания.
Продукция КРФ зависит от уровня эстрогенов (женских половых
гормонов). Во время менструации (месячных) уровень эстрогенов
снижается, а уровень КРФ повышается, что обуславливает обострение
воспалительного процесса. Кроме того, менструальная кровь содержит
большое количество железа, необходимого для жизнедеятельности
паразита, что также вносит "посильный вклад" в развитие болезни
(необходимо отметить также, что избыточное количество ионов железа
тормозит активность защитных белков организма, ответственных за
"борьбу" с трихомонадой). При местном применении эстрогенов
(гормональные препараты, противозачаточные таблетки) уровень КРФ
снижается, а клинически отмечается некоторое улучшение в течении
заболевания.
 |
|
Фагоцитоз (поглощение) трихомонадой гонококков (Gn) |
Таким образом, трихомонадная инфекция не приводит к развитию
выраженного иммунитета. Выявленные у больных или переболевших
трихомониазом лиц антитела являются лишь свидетелями существующей
или перенесённой инфекции, но не способны обеспечить стойкий
иммунитет. Реинфекция (повторное заражение) T.vaginalis у
человека не вызывает иммунной защиты.
Урогенитальная трихомонада
как моноинфекция встречается только у 10,5% больных трихомониазом,
а его смешанные формы в ассоциациях с другими инфекциями
передаваемыми половым путем наблюдаются у 89,5% пациентов.
Трихомонады могут быть ассоциированы с микоплазмами (47,3%);
гонококками (29,1%); гарднереллами (31,4%); уреаплазмами (20,9%);
хламидиями (18,2%) и грибами (15,7%).
Особого
внимания заслуживает общебиологический феномен - способность
влагалищных трихомонад к захвату и резервированию различных
патогенных и условно-патогенных микроорганизмов. В таких случаях
воспалительный процесс приводит к выраженной реакции тканей, что
сопровождается повреждением, деструкцией и дисплазией эпителия. При
микст-инфекции (смешанной инфекции), в условиях снижения иммунитета и выраженном
воспалительном процессе, развиваются кровоизлияния, повреждаются
слои гладкой мускулатуры, прилегающие непосредственно к пораженной
слизистой оболочке, образуются грануляции (разрастания ткани).
Способность урогенитальных трихомонад к фагоцитозу (поглощению)
гонококков, хламидий, микоплазм, грибов и вирусов способствует
количественному уменьшению последних в половых путях, что может
приводить к снижению антигенного и токсикогенного воздействия на
организм, уменьшению фагоцитарной реакции и снижению иммунного
ответа организма на инфекционный фактор.
Способность урогенитальных трихомонад к фагоцитозу (поглощению)
гонококков, хламидий, микоплазм, грибов и вирусов способствует
количественному уменьшению последних в половых путях, что может
приводить к снижению антигенного и токсикогенного воздействия на
организм, уменьшению фагоцитарной реакции и снижению иммунного
ответа организма на инфекционный фактор.
Забегая вперед, отметим, что безуспешность лечения той или иной
урогенитальной инфекции часто бывает обусловлен тем, что данный
инфект находится внутри поглотившей его трихомонады, а значит и
недоступен для большинства препаратов.
Хотя в настоящее время многими исследователями недооценивается роль
влагалищных трихомонад в патогенезе сохранения и рецидиве ИППП.
Следствием чего часто является "слепая" (без должного лабораторного
контроля и анализа данных) массивная антибиотикотерапия, приводящая
к увеличению в популяции удельного веса такого полиэтиологического
синдрома, как бактериальный вагиноз (гарднереллез). Различные
нарушения состава микрофлоры, в свою очередь, резко увеличивают
длительность бактерионосительства.
Необходимо отметить, что в содержимом половых путей у больных
трихомониазом женщин практически никогда не определяются
лактобациллы, которые служат биологическим "барьером" для роста и
распространения условно-патогенной микрофлоры и являющиеся одним из
основных критериев нормоценоза.
Помимо общеизвестного механизма бактерицидного действия лактобацилл,
который заключается в расщеплении ими гликогена влагалищных
эпителиальных клеток с высвобождением молочной кислоты, а также
образовании перекиси водорода, препятствующих размножению анаэробных
и других микроорганизмов во влагалище, лактобациллы обладают
выраженной лизоцимной активностью, определяющей их антагонистическое
действие по отношению к условно-патогенной микрофлоре.
Лабораторная диагностика.
Диагностика урогенитального трихомониаза основывается на выявлении
клинических признаков заболевания и обнаружении в исследуемом
материале T.vaginalis.
В
связи с тем, что клинические симптомы довольно часто не отражают
реальной картины заболевания, в обязательном порядке необходимо
применение лабораторных методов диагностики.
 |
|
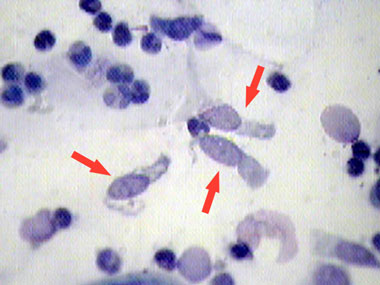
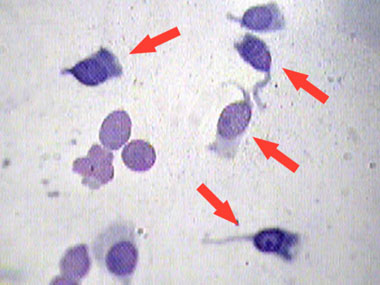
Мазок из уретры (окраска метиленовой
синькой): трихомонады показаны стрелками |
|
В настоящее время в России и за
рубежом применяют четыре лабораторных метода определения
Trichomonas vaginalis: микроскопический, культуральный,
иммунологический и генодиагностический
(молекулярно-биологический).
Микроскопический
метод включает две методики.
Первая - это
определение трихомонад в нативном препарате при фазовом
контрастировании. Необходимо найти овальное или грушевидное
тело, чуть больше лейкоцита, имеющее жгутики и совершающее
характерные толчкообразные поступательные движения. Такое
исследование следует делать практически “не отходя от пациента”,
иначе в течение нескольких минут влагалищная трихомонада может
прекратить свои движения.
Вторая методика
- это окрашивание препарата метиленовым синим (как вариант:
раствором бриллиантовой зелени) или по Граму. Ведётся поиск
известной формы трихомонады с правильно очерченным асимметричным
ядром на фоне нежно ячеистой структуры цитоплазмы.
Для
выявления жгутиков и ундулирующей мембраны препарат следует
окрашивать по Романовскому-Гимзе.
Чувствительность метода микроскопии по данным литературы
варьирует от 38% до 82%. Несмотря на то, что этот метод среди
диагностических тестов является определённо экономически
наиболее целесообразным и простым, он имеет низкую
чувствительность и специфичность. Это может быть обусловлено, в
первую очередь, потерей трихомонадами характерной подвижности
после того, как простейшее уже извлечено из среды человеческого
организма. Особенно большая доля субъективизма проявляется в
случае препаратов с низким титром или препаратов, содержащих
огромное количество клеток эпителия, лейкоцитов и различного
деструктивного материала из очага поражения. В очаге поражения
влагалищная трихомонада часто представлена округлыми формами,
напоминающими полиморфноядерные лейкоциты, и естественно,
типичные морфологические признаки теряются во время фиксации и
окрашивания, создавая трудность для этиологической
идентификации.
Метод выращивания
трихомонад в бульонной культуре - "золотой стандарт" для
диагностики, потому что это простой в интерпретации метод и
требует менее, чем 300-500 трихомонад/мл инокулюма (забранного
материала) для начала роста в культуре. Тем не менее, для него
существуют ограничения, присущие культуральным методам. Для
диагностики необходим инкубационный период от 5 до 7 дней,
являющийся слишком длительным из-за возможности инфицированного
пациента к распространению инфекцию. В связи с этим он не
получил широкого применения в клинической практике в качестве
прямого диагностического метода.
Для
улучшения восприятия культурального метода, за рубежом был
разработан метод пластикового конверта, с помощью которого можно
выполнить как немедленную проверку присутствия трихомонады, так
и сохранить дальнейший рост трихомонад в одной
самоподдерживающейся системе. Полученные результаты сравнимы с
таковыми при исследовании мазка и культур. Аналогично
пластиковому конверту используется система InPouch в виде
двухкамерного мешка, позволяющая выполнить быструю проверку
культуры путём микроскопии через стенку мешка.
В России
культуральный метод (или, бакпосев) широко используется в
лабораторной диагностике трихомониаза. Проведенный в 1990 г.
анализ качества диагностики трихомониаза в ЦНИКВИ МЗ РФ,
показал, что подавляющее число больных трихомониазом (72,8%) как
среди женщин, так и среди мужчин были выявлены при
использовании именно культурального метода. Из отечественных
стандартных сред, не уступающих по качеству зарубежной среде
Джонсона-Трассела, можно рекомендовать в практическое
здравоохранение среду СКДС или среду М.М.Васильева, которая дает
99,7% положительных результатов выявления урогенитальных
трихомонад из патологического отделяемого слизистых мочеполового
тракта.
Состав среды Джонсона-Трассела: 20% печеночного настоя, 20% человеческой сыворотки, 2% пептона, 0,1%
мальтозы, 0,15% солянокислого цистеина, 60% раствора Рингера
(натрия хлорида – 6,5 г, калия хлорида – 0,14 г, кальция хлорида
– 0,12 г, натрия гидрокарбоната – 0,2 г, все это доводится до 1
л дистиллированной водой) и 0,0002% метиленового синего; pH
среды 6,0 – 7,5 ; температура 37-39 С°.
Состав СКДС:
100 мл солевого раствора (натрия хлорида 6,5 г, калия хлорида
0,14 г, кальция хлорида 0,12 г, натрия бикарбоната 0,2 г, 0,2%
раствора метиленового синего 0,5 мл, дистиллированной воды 1 л);
10 мл гидролизата казеина для парентерального белкового питания;
10 мл дрожжевого аутолизата; 30 мл сыворотки крови лошади или
крупного рогатого скота без консерванта; 10 мл 20% раствора
мальтозы; пенициллина и стрептомицина по 100 000 ед.
Среду разливают в стерильные пробирки по 5 мл, заливая их слоем
стерильного вазелинового масла толщиной 5 мм. Посев производят,
помещая исследуемый материал на дно этих пробирок.
Урогенитальные трихомонады дают придонный рост в виде плотного
беловатого осадка, из которого пастеровской пипеткой берут
материал для исследования в нативном препарате. В поле зрения
урогенитальные трихомонады могут быть одиночными или
располагаться большими скоплениями, наблюдаются активные
движения жгутиков и ундулирующей мембраны. Микроскопическое
исследование культур производят на 3-5 день, при отрицательных
результатах на 7-9 день или 11-17 день после посева, так как
длительность цикла развития урогенитальных трихомонад зависит от
величины посевной дозы.
Среда Васильева:
белковый порошок (ТУ-62-3-204-84), получаемый из отходов
производства фармацевтической промышленности при изготовлении
лизоцима.
Ограничения
культуральных и микроскопических методов для выявления
T.vaginalis заставили учёных развивать альтернативные
методы, которые могут определять антиген, антитело или
нуклеиновые кислоты в уретральном или вагинальном экссудате(воспалительной
жидкости).
Существует восемь
известных серотипов T.vaginalis. Однако иммуноблот
показывает широкое варьирование антигенных маркёров.
Используются различные методы определения антитрихомонадных
антител: агглютинация, фиксация комплемента, непрямая
гемагглютинация, диффузия в геле, флюоресценция антител и
иммуноферментный анализ.
Прямой иммуноферментный и иммунофлюоресцентный анализ мазков
вагинального соскоба, например, коммерческий метод фирмы
California Integrated Diagnostics, Benicia, Calif., использующий
пероксидазо- и флюорохром- меченные смеси моноклональных антител
к различным структурам T.vaginalis был таким же
чувствительным и специфическим, как и используемый культуральный
метод. К тому же результаты определения возбудителя трихомониаза
данным методом достигаются в течение одного часа, что позволяет
осуществлять контрольно-диагностическую функции.
С начала 90-х годов
в лабораторную клиническую практику стали внедрятся технологии
определения видоспецифических нуклеотидных последовательностей
областей ДНК (мишеней) геномов вирусов, бактерий и клеток высших
организмов.
Новая
генодиагностическая технология - “ПЦР-технология” (ПЦР –
полимеразная цепная реакция) в последнее время опережает
остальные методы генодиагностики трихомониаза и наравне с
культуральным методом широко используется в клинической
практике. Суть методики состоит в определении наличия "кусочков"
ДНК определяемого возбудителя во взятой среде. К сожалению,
практический опыт показывает, что перспективы определения
трихомонад методом ПЦР не столь радужны, как они описываются в
литературе. По нашим данным, примерно половина анализов дают
ложноотрицательный результат, по сравнению с культуральным
методом. Очевидно, пока это связано с несовершенством методики.
Клиника.
Клинические проявления трихомонадной инфекции отличаются большим
разнообразием, от острых форм с выраженной клиникой до
малосимптомного или бессимптомного течения заболевания.
Урогенитальный (мочеполовой) трихомониаз может протекать в виде
моноинфекции, смешанной или сочетанной инфекции.
Смешанная инфекция
подразумевает заболевание, вызванное одновременно двумя или более
возбудителями. Сочетанная инфекция – “это последовательное
развитие двух или более инфекционных болезней, причем их
максимальные проявления могут наблюдаться как в одном, так и в
разных органах” (Серов В.В., 1995г.). Моноинфекция подразумевает в
качестве причины возникновения болезни наличие только одного
патогенного возбудителя.
Также, выраженность клинических проявлений заболевания зависит и от
реактивности (способности реагировать на микроб) организма,
состояния его иммунитета.
У
одних (чаще молодых и чаще при первичном заражении) людей
трихомониаз проявляется в виде зуда, умеренных или обильных
прозрачных слизистых выделений из половых путей через короткое время
после заражения. Прогноз заболевания при своевременном и адекватном
лечении, как правило, благоприятен. Излечение происходит в короткие
сроки и сравнительно небольшими дозами препаратов.
У
других, мочеполовой трихомониаз может протекать годами, не доставляя
особого беспокойства (так называемые случаи "семейного
трихомониаза"). У этой категории больных трихомонады чаще выявляются
скорее случайно при "плановом" обследовании и лечении какой-нибудь
хронической болезни наподобие простатита или аднексита. В таких
случаях выявление возбудителя происходит, скорее, благодаря
дотошности и опыту врача. При сборе анамнеза (истории развития
заболевания) иногда удается выяснить, что сам пациент когда-то
отмечал у себя вышеописанные или похожие симптомы, которые со
временем сами собой прошли и забылись.
Еще одну
категорию составляют лица, у которых произошло повторное (иногда
неоднократное) заражение. Клиника при этом может быть стертая, не
выраженная. Поэтому сами пациенты могут и не подозревать о наличии у
них продолжающегося трихомониаза, который протекает в данном случае
в виде так называемого трихомонадоносительства. Для своих половых
партнеров они, как и предыдущая группа больных, представляют
опасность в качестве источника заражения.
Для
правильного назначения лечения большое практическое значение имеет
вопрос о классификации трихомониаза. В основу классификации
положена интенсивность реакции организма на внедрение урогенитальных
трихомонад, отражением которой является клиническое проявление
болезни. С этой точки зрения целесообразно различать следующие
формы:
- свежий (не
более 2 мес)
-
острый (<
2 нед)
-
подострый (2-4 нед)
-
торпидный
-
хронический
-
трихомонадоносительство (латентная форма)
При любой форме урогенитального трихомониаза в воспалительный
процесс могут вовлекаться абсолютно все органы мочеполовой системы,
а также нижние отделы кишечного тракта. Появляется все больше
сообщений о трихомонадных проктитах (воспаление прямой кишки),
тонзиллитах и др. Однако характерным является вовлечение в
воспалительный процесс определенных органов мочеполовой системы в
зависимости от возраста пациента и физиологического состояния.
Поэтому также существуют классификации, основанные на локализации
воспалительного процесса.
-
Урогенитальный трихомониаз нижних отделов мочеполовой системы:
-
вульвит
-
кольпит
-
экто- и эндоцервицит
-
уретрит
-
бартолинит
-
баланопостит
-
Урогенитальный трихомониаз органов малого таза и других отделов
мочеполовой системы:
-
эндомиометрит
-
сальпингит
-
сальпингоофорит
-
эпидидимит
-
цистит
-
простатит
-
везикулит
-
Трихомониаз других локализаций (фарингит, тонзиллит, проктит и
др.)
Однако с практической точки зрения локализация трихомониаза -
вопрос времени, так как по мере увеличения длительности заболевания
распространенность поражения увеличивается. Поэтому для врача она
имеет часто вспомогательное значение.
Трихомониаз у мужчин.
Перед дальнейшим прочтением рекомендуется ознакомится с анатомией
мужского мочеполового тракта (мочеполовая
система,
малый таз,
простата,
пенис)
При заражении трихомониазом у мужчин первично инфицируется эпителий
слизистой оболочки ладьевидной ямки передней (пенальной, или
стволовой) уретры. Трихомонады, активно двигаясь, распространяются
по слизистой передней уретры, а примерно через 2 недели проникают в
заднюю (простатическую) часть уретры.
Распространение возбудителя по уретре сопровождается поражением
парауретральных желез (Литтреевских, Скане, крипт Морганьи), которые
анатомически представляют из себя своего рода "кармашки".
Физиологическая Функция этих желез заключается в выделении слизи,
препятствующей высыханию слизистой оболочки уретры и препятствию
слипания ее стенок. В норме количество слизи незначительное. При
поражении этих желез инфектом, в том числе и трихомонадой, возникает
их воспаление (литтреиты, морганиты), которое сопровождается
обильным выделением слизи. Именно этим обусловлено наличие обильного
отделяемого из наружнего отверстия уретры у заболевшего. Слизь
раздражает поверхностную оболочку мочеиспускательного канала,
поэтому больные отмечают также и зуд.
Адекватное и своевременное лечение элиминирует (уничтожает)
возбудителя и купирует болезненные симптомы. Однако в случае его
отсутствия или неадекватности организм в некотором роде
"приспосабливается" к болезни, и трихомониаз получает свое
дальнейшее развитие. Острота процесса снижается, постоянное
слизеотделение и зуд уменьшаются или исчезают вовсе. Наступает
период мнимого благополучия. Трихомонады постепенно "заселяют"
парауретральные железы, которые в свою очередь, становятся
хроническими очагами инфекции. В просвет уретры трихомонады попадают
только в случае "опорожнения" такой железы (например, при половом
сношении). Они поражают соседние железы, в том числе и Куперовы
(соответственно, вызывая их воспаление – Куперит, который может
сопровождаться болями в промежности). Постепенно воспаление
распространяется на простатическую часть уретры, вовлекая в процесс
семенной бугорок, ацинусы предстательной железы (железки,
продуцирующие простатический сок), семенные пузырьки (продуцируют
секрет, являющийся своеобразным "топливом" для сперматозоидов,
отсюда и частое бесплодие при трихомониазе), семяпроводы (по которым
возбудитель проникает в яички), а также слизистую мочевого пузыря и
верхних мочевых путей.
|
 |
 |
|
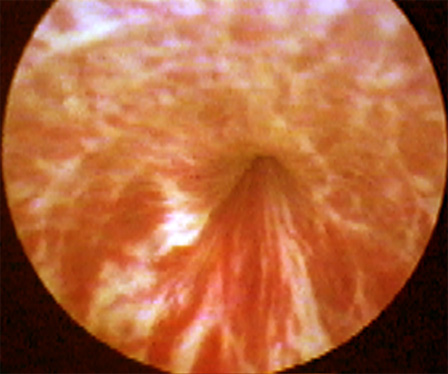
Нормальная
эндоскопическая картина наружнего мочевого сфинктера |
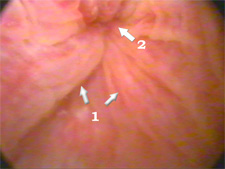
Инфильтративный отек
складок слизистой (1), сходящихся к отверстию
сфинктера(2) |
По
данным ряда авторов, трихомонадный уретрит у мужчин в 30% случаев
протекает в острой форме, в 60-70% - в хронической или бессимптомно.
У 30-50% больных диагностируются осложнения в виде простатитов,
везикулитов, эпидидимитов, баланопоститов.
Вышеописанное характерно не только для трихомонад, но и
для других уретральных инфекций, только степень патологических
изменений будет различаться в зависимости от вида возбудителя и
вирулентности (агрессивности) его штамма (разновидности).
Для трихомонадной инфекции часто характерно образование
инфильтратов. Вероятность их образования возрастает с длительностью
самого заболевания, а также зависит от реактивности
организма-хозяина.
Большую роль в этом
играет вышеупомянутый белок –
клеточный
разъединяющий фактор (КРФ). Именно при помощи него
трихомонады в ассоциации с другими микробами внедряются в толщу
тканей мочеиспускательного канала и образуют там своего рода
"колонии", защищенные от неблагоприятных внешних воздействий
(изменений кислотности среды, лекарственных препаратов и др.).
Исходом таких инфильтратов могут быть язвы, рубцы, иногда грубо
нарушающих нормальное функционирование мужского мочеполового
аппарата.
|
 |
|
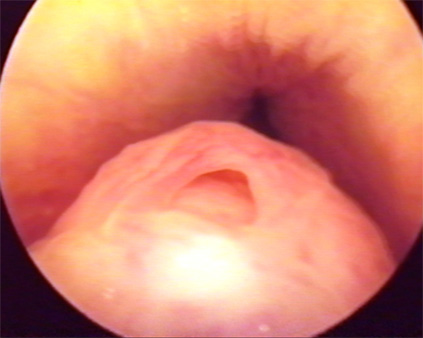
Нормальная
уретроскопическая картина семенного бугорка
("кармашек" в центре – мужская
маточка) |
|
Жалобы могут разниться в зависимости от локализации инфильтрата.
При поражении передней уретры мужчины жалуются на некоторое
затруднение при мочеиспускании. Это связано с механическим
препятствием, обусловленным отеком слизистой и уменьшением просвета
канала. При инфильтратах задней уретры ( часто это инфильтрат
семенного бугорка), может отмечаться типичный болевой синдром
больного хроническим простатитом, гемоспермия (выделение крови при
эякуляции) или уретроррагия (выделение крови из наружнего отверстия
мочеиспускательного канала). Это связано с повышенной ранимостью
пораженных тканей. При проникновении
трихомонад в просвет семенных
пузырьков инфект обедняет их секрет, используя для своей
жизнедеятельности питательные вещества (лактоза, фруктоза и др.),
необходимые для поддержания жизнеспособности сперматозоидов в
эякуляте (по данным исследований 75% объема нормального эякулята
составляет сок простаты, до 20% - секрет семенных пузырьков и лишь
5% - сперматозоиды). Это, в свою очередь, может являться причиной
бесплодия. Отек и механическое сдавление устьев семявыбрасывающих
протоков (туда открываются выводные протоки семяпроводов и семенных
пузырьков) вызывает болевые ощущения при эякуляции.
Для диагностики (кроме
общепринятых, рутинных методов исследования) трихомонадных поражений
нижних отделов мочеполового тракта используется специальный метод
исследования, называемый уретроскопией. Другие инструментальные
методы исследования в данной ситуации мало информативны.
Уретроскопия позволяет точно определить место и характер поражения,
а также адекватно проводить в дальнейшем так называемое "местное"
лечение в виде различного вида механического или лекарственного
воздействия на очаг поражения.
 |
 |
|
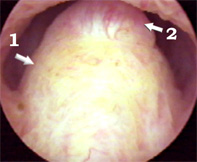
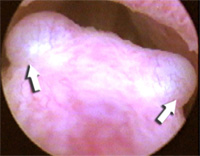
Трихомонадный инфильтрат
(2), расположенный на семенном бугорке (1) |
Трихомонадные
инфильтраты (показаны стрелками) |
Трихомониаз у женщин.
Перед дальнейшим прочтением рекомендуется ознакомится с
анатомией женской половой сферы (малый
таз,
матка,
вульва).
Заболевание, как известно, протекает с поражением нескольких
топических очагов мочеполовой системы, а ряде случаев в
воспалительный процесс вовлекается ампула прямой кишки.
Мочевыделительная
система может инфицироваться на всем протяжении – от уретры до
паренхимы почек, хотя в большинстве случаев диагностируется уретрит
и реже цистит.
Половая система женщин
может также подвергаться заражению на всем протяжении - от вульвы
(преддверия влагалища) до яичников и далее по протяжению до брюшины,
но преимущественно воспаление ограничивается внутренним зевом шейки
матки. При осмотре обнаруживают явления вульвита, кольпита, экзо – и
эндоцервицита.
Трихомонадный вульвит
(поражение больших и малых половых губ, клитора, остатков
девственной плевы, задней спайки - вульвы) характеризуется
отечностью и гиперемией (покраснением) тканей, иногда выявляются
расчесы, очаговое покраснение кожа вокруг, гнойнички, эрозии и
язвочки. Половая близость вызывает боль в области входа во
влагалище. Раздражение этой области выделениями из половых путей
вызывает образование экземы. Вульвиты часто сочетаются с
бартолинитами (воспалением Бартолиниевой железы, или железы
преддверия влагалища) и, как правило, с кольпитами.
При остром
трихомонадном кольпите (воспаление стенок влагалища)
появляются жалобы на обильные, жидкие, часто пенистые,
бледно-желтого или желтоватого цвета бели, зуд и жжение в области
половых органов и дизурические явления. При пальцевом и
инструментальном исследовании влагалища выявляется разрыхленность и
легкая кровоточивость ее стенок. В отдельных случаях на слизистой
оболочке наблюдаются возвышающиеся красные пятна величиной с
булавочную головку, а также мелкие поверхностные язвы.
Если эти язвы не лечить, они дают осложнения в
виде слоновости, что в начале XX века трактовалось как эстиомен
вульвы (estiomene
vulvae). Те
хирургические иссечения язв на фоне слоновости приводили к сильным
рубцовым изменениям с последующим рецидивом язвенного процесса, так
как не применяли противоцистоидного воздействия на виновника этого
процесса – урогенитальной трихомонады. При дальнейшем развитии этого
воспалительного заболевания, спустя 8-10 лет происходила
трансформация длительно текущего заболевания в рак Педжета.
В зависимости от выраженности тех или иных
клинических проявлений острый трихомонадный кольпит может быть
простым макулезным, гранулезным, язвенным, а также смешанным.
Наблюдается усиление
транссудации (продукции жидкости) в патологически измененной стенке
влагалища; отделяемое из него может быть серозным, серозно-гнойным,
крошковидным. Выделений иногда так много, что они заполняют оболочки
влагалища, задний влагалищный свод, причем влагалищная часть шейки
матки как бы "купается" в них. Количество, цвет, запах и
консистенция белей зависят, очевидно, от численности состава
трихомонад, сопутствующей бактериальной флоры и реактивности
организма, которая нередко может изменяться под влиянием
беременности, абортов и других вмешательств.
При хроническом
трихомонадном кольпите клиническая картина не имеет
резко выраженных признаков, и заболевание нередко выявляется как
довольно случайная находка при очередном профилактическом осмотре.
Жалобы, которые обычно присущи острым и подострым формам
урогенитального трихомониаза, могут отсутствовать или проявляться в
виде небольшого зуда, исчезающего при тщательном проведении
гигиенических мероприятий и усиливающегося в предменструальный и
послеменструальный периоды.
У некоторых больных
воспалительная реакция трихомонадной этиологии (происхождения)
способна распространяться не только на нижние отделы половых
органов, но и на шейку матки (экзоцервицит, или цервицит), и
шеечный канал (эндоцервицит). Клинически цервицит протекает главным
образом по типу хронической, реже – подострой воспалительной
реакции. При этом на шейке матки отмечается гиперемия, отечность
тканей, эрозии и язвы слизистой.
При эндоцервиците
(воспаление канала шейки матки) слизистая отечна, разрыхлена,
нередко кровоточит, а выделения носят слизисто-молочный или
слизисто-гнойный, иногда пенистый характер.
Следует отметить, что цервициты никогда не
протекают изолированно от кольпитов, поэтому и клинические
проявления его аналогичны таковым при кольпите.
Внутренний зев шейки
матки является как бы границей распространения урогенитальных
трихомонад вверх. Этому служит циркулярное сжатие мускулатуры шейки
матки, с одной стороны, а с другой – резкая щелочность секрета
эндометрия. Эти защитные моменты в известной мере теряют свою силу
во время менструации, абортов и родов. Кроме этого, ритмическое
движение матки во время полового акта является способствующим
моментом "всасывания" урогенитальных трихомонад, находящихся в шейке
матки, в ее полость. Возникает трихомонадный эндометрит.
На слизистой оболочке
матки урогенитальные трихомонады находятся временно, вызывая отек,
набухание, перерождение эндометрия. Острый эндометрит проявляется
увеличением количества белей, нередко с примесью крови, появлением
болей внизу живота, которые могут быть объяснены плохим оттоком
секрета, застаивающегося в полости матки. Наступает расстройство
менструаций (их обилие и нерегулярность).
При проникновении
урогенитальных трихомонад в маточные трубы возникает
трихомонадный сальпингит. Этому способствуют усиленные
сокращения маточной мускулатуры, повышенное внутриматочное давление
при закупорке маточных труб накопившемся воспалительным секретом
эндометрия. Клинически это выражается появлением болей внизу живота,
более резко выраженных в одной половине. При прогрессировании
воспалительного процесса абдоминальный (открывающийся в просвет
брюшной полости) конец трубы закрывается вследствие склеивания
ворсинок между собой и соседними органами – яичником и широкой
фасцией матки. Продолжающаяся секреция (продукция жидкости)
растягивает стенки трубы. Эти стенки пальпируются в виде тяжа;
больные жалуются на боли в крестце и внизу живота, усиливающиеся во
время менструации.
Кульминацией
трихомонадный поражений женской половой сферы является оофорит,
или воспаление яичников. Поскольку их поражение – следствие
воспаления в маточных трубах, то чаще говорят о сальпингоофорите.
Простейшие из просвета
маточной трубы распространяются на поверхность яичника, разрушая его
нежный зачатковый эпителий. Возникающий воспалительный экссудат
(жидкость с примесью защитных белков) покрывает всю поверхность
яичника, который постепенно превращается как бы в капсулу.
Образующиеся рубцы могут сдавить придаток, нарушают питание в нем,
ведущее к атрофии органа и преждевременному прекращению его функции.
Трихомонады, проникая внутрь яичника, могут вызвать образование
мелких гнойников. Иногда между перепонками, соединяющими трубу с
яичником, возникают тубоовариальные кисты, наполненные серозной
жидкостью.
Кроме того, процесс
затрагивает еще одну деликатную ткань, а именно брюшину (тонкая
пленка, покрывающая изнутри все внутренние органы) в ее тазовом
отделе. При этом возникает так называемый хронический тазовый
перитонит. Последствия ее воспаления наиболее полно проявляются
спаечным процессом в малом тазу с образованием обширных спаек между
соседними органами: маткой, маточными трубами, яичниками, прямой
кишкой. Результатом является неблагоприятное влияние на нормальную
функцию яичников, что может проявляться преждевременным или
замедленным созреванием яйца или прекращением его созревания. Это
приводит к учащению или замедлению менструаций, вплоть до полного их
прекращения. С другой стороны, из-за плохой проходимости маточных
труб затрудняется выход созревшего яйца в полость матки, что может
привести к стерильности больной женщины.
Поражения
трихомонадами уретры и мочевого пузыря у женщин
сопровождаются патологическими изменениями тканей, аналогичными у
мужчин. Клиника характеризуется в основном зудом в уретре и дизурией
(боли и рези при мочеиспускании, позывы на мочеиспускание, чувство
неполного опорожнения мочевого пузыря, частые микции и т.д.)
Затекание содержимого
половых путей в область анального отверстия может вызвать
проникновение трихомонад в прямую кишку и возникновение
трихомонадного проктита. Он характеризуется в основном тенезмами
(позывами на дефекацию).
Общепринятые методики
забора клинического материала позволяют исследовать образцы,
полученные из уретры, наружных половых органов, нижнего отдела
внутренних половых органов и ампулы прямой кишки.
Таким образом,
лабораторная диагностика трихомонадной инфекции вышележащих отделов
половой и мочевыделительной систем становиться возможной с
использованием специальных урологических и гинекологических методик
обследования. Диагноз трихомонадного цистита, эндомиометрита и т.д.
устанавливается на основании жалоб и данных объективного осмотра,
являясь по существу клиническим. Для подтверждения этиологической
роли влагалищной трихомонады в развитии данной патологии необходимо
выделить возбудитель непосредственно из отделяемого инфицированных
органов. Следует подчеркнуть, что подобные манипуляции в условия
дерматовенерологической службы не проводятся, и, следовательно,
диагноз, например, “трихомонадный эндомиометрит” является достаточно
условным с точки зрения этиологии воспалительного процесса. По-
видимому, именно в этой связи в доступной литературе отсутствуют
реальные показатели инфицирования влагалищной трихомонадой
вышележащих отделов мочеполовой системы.
Изолированное поражение
того или иного участка мочеполовой системы наблюдается крайне редко.
Трихомонады наиболее часто выявляются в
цервикальном канале (81%), реже – в уретре (62%), влагалище – (18%),
крайне редко – в ампуле прямой кишки (5%) У 93% обследованных женщин
трихомонады обнаружены в уретре.
Как было установлено, у
женщин репродуктивного возраста вне беременности наиболее часто
поражается цервикальный канал, уретра и влагалище. Значительно реже
воспалительный процесс охватывает органы мочевыделительной системы,
лежащие выше сфинктера мочевого пузыря и органы половой системы,
расположенные выше внутреннего маточного зева, а также ампулу прямой
кишки.
Трихомонадная инфекция у беременных женщин
многоочаговое заболевание - инфицируется уретра, нередко мочевой
пузырь, вульва, влагалище и прямая кишка. Возможность трихомонадной
инвазии внутренних половых органов зависит от срока беременности, в
который произошло инфицирование. Все анатомо-физиологические
процессы, происходящие во время беременности, направлены на защиту
плода от восходящей инфекции. Резко возрастает активность
материнских иммунных механизмов, включая стимуляцию фагоцитарного
ответа. С самых ранних сроков беременности формируются
дополнительные защитно-биологические барьеры. В первую очередь
меняется характер цервикальной слизи, она становится вязкой, трудно
проходимой для инфекционных агентов. Начиная с 16-ой недели,
функционирует второй барьер – хориоамнионические оболочки, которые
закрывают внутренний маточный зев канала шейки матки. Если заражение
произошло до формирования хориоамниотических оболочек, вероятность
восходящего пути распространения инфекции достаточно велика,
развивается трихомонадный эндомиометрит. Беременность в таком случае
в большинстве наблюдений прерывается в результате самопроизвольного
выкидыша. Если заражение трихомониазом произошло позже, восходящая
инфекция развивается редко, и своевременно назначенная специфическая
терапия приводит к клинико-этиологическому излечению, нормальному
течению беременности, родов и послеродового периода.
Принципы лечения урогенитального трихомониаза.
До 1959 года местные
вагинальные препараты, включая лекарственные средства принятые в
народной медицине, воздействующие на трихомонаду, давали
незначительное улучшение при определённых клинических проявлениях
болезни, но не вызывали полного уничтожения (эрадикации) паразита в
мочеполовых путях человека. Применяемые в то время препараты не
санировали эпителий влагалища и уретры, бартолиниевые железы и
простату, которые были основной средой обитания возбудителя
трихомониаза. Даже если женщины лечились успешно, то их половые
партнёры ввиду скудности клинической симптоматики, как правило, не
лечились вообще или лечились недостаточно, следствием чего являлась
реинфекция.
Новая эра в терапии урогенитального трихомониаза
началась в 1959 году, когда впервые было синтезировано
нитроимидазольное производное антибитика “азомицина” из Streptomyces
- высокоэффективное синтетическое средство для лечения данного
заболевания. Полное химическое название этого антибиотика альфа,
бета-гидроксиэтил-2-метил-5-нитроимидазол под общим названием
“метронидазол” и продаваемого под торговом наименованием “Флагил”
или “Трихопол” в России. Другие нитроимидазолы разрешённые для
клинического применения в разных странах мира - это тинидазол
(фазижин, триконидазол), орнидазол (тиберал), секнидазол,
флюнидазол, ниморазол (наксоджин), карнидазол, тержинан.
В настоящее время, как
показывает практика, применявшиеся ранее "стандартные" методики
лечения, равно как и "стандартные" дозировки, рекомендованные
производителями фармпрепаратов, в большинстве случаев оказываются
малоэффективными против трихомонад и других бактерий. Причин тому
несколько.
Во первых,
бесконтрольное применение антибактериальных препаратов в нашей
стране, обусловленное их доступностью в аптечной сети (особенно
коммерческой), привело к появлению большого количества устойчивых к
этим препаратам форм бактерий.
Устойчивость влагалищных трихомонад к проводимому
лечению может быть следствием мутаций, воздействующих как на
аэробный, так и на анаэробный метаболизм. Тесты на чувствительность
in vitro для T.vaginalis лучше отражены при аэробном
культивировании, поскольку при анаэробном культивировании
наблюдается некоторое снижение чувствительности. Следует
подчеркнуть, что минимальная летальная концентрация лекарственного
вещества в сыворотке крови при анализах на чувствительность не
отражает реальную концентрацию препарата, необходимую для излечения,
но может помочь в определении дозы препарата.
Кстати, не стоит сбрасывать со счетов и такую
немаловажную деталь, как качество самого лекарственного препарата.
По некоторым данным, доля подделок среди импортных лекарств на
отечественном фармрынке составляет до 70%!
Во вторых, отсутствие
должного медицинского контроля за эффективностью лечения, например,
в результате самолечения.
В третьих, недостаточно
четкое представление о механизмах развития болезни не позволяет
применить весь доступный и целесообразный в каждом конкретном случае
арсенал лечебных средств.
Исходя из
вышеперечисленного, можно обозначить несколько основных принципов
лечения трихомониаза. Все проводимые лечебно-диагностические
мероприятия и назначаемые препараты должны быть строго обоснованы.
Проводить их следует, руководствуясь мудрым правилом "от простого к
сложному". Не стоит начинать обследование пациента с применения
дорогостоящих видов обследования (например, желательно сначала
провести микроскопию мазка из уретры или вагины, а лишь потом в
качестве уточняющих тестов проводить бакпосев, иммуноферментный
анализ (ИФА) или ПЦР-диагностику).
Как показывает
практический опыт, применение только медикаментозного лечения
эффективно лишь при острой форме трихомониаза. Поэтому, если
трихомонадная инфекция в организме существует более 2 недель, лучше
лекарственную терапию сочетать с так называемым "местным" лечением.
Оно может различаться в зависимости от пола человека, а также от
степени выраженности поражений тканей.
Предполагая у мужчин наличие длительно
протекающего трихомониаза, а значит и обсеменение не только передней
уретры, но и простаты с парауретральными железами ( железы Литтре,
Куперовы железы, семенные пузырьки), логичным будет проведение
массажа уретры на буже в сочетании с массажем простаты с последующей
инстилляцией (промыванием) уретры растворами уроантисептиков. Для
более точного представления о характере и уровне поражения
целесообразно предварительное проведение как "сухой" передней, так и
тотальной ирригационной уретроскопии. Аналогичный подход в отношении
обследования и лечения женщин. Местные манипуляции (тампонады,
спринцевания, прижигания) должны предваряться кольпоскопией с
обязательным осмотром шейки матки и сводов влагалища.
Необходимо отметить, что
обязательному лечению должен подвергаться не только пациент, но и
его половой партнер, независимо от того, есть ли у него симптомы
заболевания или нет. Только так можно избежать повторного заражения
в будущем.
Для медикаментозного
лечения трихомониаза применяются препараты нитроимидазольной группы:
тинидазол (фазижин, триконидазол),
орнидазол (тиберал), секнидазол, флюнидазол, ниморазол (наксоджин),
карнидазол, тержинан. Схемы приема и
дозировки препаратов у различных специалистов могут отличаться от
рекомендованных производителем, что определяется личном опытом
врача. Медикаменты могут применяться как в таблетированной форме,
так и в растворах (например, метрогил), в вагинальных таблетках
(например, "Клион"-Д) или свечах (суппозиториях).
Нитроимидазолы проходят через плацентарный барьер
и, хотя врождённые аномалии плода в настоящее время не связываются
непосредственно с их потреблением, имидазолы всё-таки не показаны
для применения у женщин в первом триместре беременности. Большинство
российских и зарубежных авторов считают, что риск появления
врождённых дефектов у плода после употребления имидазолов больными
матерями в период беременности незначителен.
Беременные, имеющие
выраженные симптомы заболевания, могут лечиться суппозиториями с
клотримазолом в дозе 100 мг интравагинально на ночь в течение 6-12
дней. Этим методом излечение достигается в 50% случаев. При наличии
клинической картины болезни и необходимости дальнейшего лечения, его
надо задержать, по крайней мере, до наступления второго или третьего
триместра беременности и провести противотрихомонадный курс по одной
из общепринятых схем.
Лечение женщин, кормящих грудью, осуществляется, в основном,
интравагинальными средствами, а прием внутрь нитроимидазольных
препаратов желательно проводить после полного прекращения
естественного вскармливания.
Эмпирическим путем найдено, что лечение
трихомониаза гораздо эффективнее, если с имидазолами применяется еще
один лекарственный препарат. Обычно это либо антибиотик широкого
спектра действия (Зитролид, Зи-фактор, Доксициклин и др.), либо один
из фторхинолонов нового поколения (Таваник и др.) Данный феномен
можно объяснить тем, что имеющаяся сопутствующая микрофлора
поглощает часть противотрихомонадного препарата, если тот
применяется в качестве монотерапии. А это существенно снижает его
концентрацию в тканях.
Проведение специфической
иммунотерапии вакциной “Солкотриховак” у женщин и “Солкоуровак”
("Уротрих") у
мужчин позволяет снизить удельный вес рецидивов заболевания и
обязательно показано при торпидном и хроническом течении болезни.
Введение вакцины солкотриховак (женщины) или солкоуровак (мужчины)
проводится внутримышечно: 3 инъекции с интервалом 2 недели между
каждой инъекцией.
Вакцина представляет из себя инактивированные
лиофилизированные микроорганизмы штамма ацидофильных лактобацилл. В
1 дозе вакцины содержится 75х109 бактерий. В 1 упаковке
находится флакон с порошкообразной вакциной и 0,5 мл растворителя.
Непосредственно перед применением компоненты смешивают.
Неспецифическая
иммунотерапия может проводится назначением различных препаратов,
повышающих общий иммунитет. Такими препаратами могут являться:
левамизол(декарис), тималин, продигиозан, Лидаза, метилурацил,
пентоксил, калия оротат, экстракт алоэ, ФиБС, стекловидное тело и
др. Выбор препаратов обычно определяется лечащим врачом. Применение
пирогенала желательно все-таки ограничить в виду того, что он
вызывает выраженную пирогенную (температурную) реакцию, изнуряя и
без того ослабленный организм пациента.
Местное лечение
при осложненных формах
трихомониаза применяется только в составе комплексного. Его вид и
объем зависят от пола пациента, выраженности тех или иных
болезненных признаков.
Мужчинам проводят массаж
уретры на буже (в мочеиспускательный канал вводят металлическую
трубку и разминают на ней уретру подобно сигарете). Этим достигается
раскрытие устьев парауретральных желез и их опорожнение, а также
усиление местного кровотока с доставкой большего количества
лекарственного вещества к очагу поражения. Те же цели достигаются
при массаже простаты.
Обычно после массажа
рекомендуется провести инстилляцию уретры раствором уроантисептика
(слабые растворы серебра, хлоргексидин, диоксидин, метрогил и др.).
Этим достигается местная санация очага поражения. В заднюю уретру
раствор можно провести мимо наружнего (мембранозного) сфинктера
только при помощи катетера. Поскольку риск повредить при этом стенку
уретры очень велик, то манипуляция должна проводиться только опытным
врачом. Наряду с инстилляциями часто применяют тампонады по
Вашкевичу. Суть манипуляции состоит в установке ватного тампона
(фактически представляет из себя свитую из ваты как из пряжи нить),
пропитанного лекарственным препаратом (бальзам Шостаковского, 2%
раствор протаргола на глицерине и др.) в переднюю уретру при помощи
уретроскопа Валентино. Через некоторое время (обычно15-20 минут)
тампон извлекается врачом или вымывается самостоятельно при
мочеиспускании.
У женщин практикуются
теплые сидячие ванночки при вульвите с растворами жидкости Бурова,
квасцов. При остром вагините назначают антисептические спринцевания,
а при стихании процесса на ночь вводят во влагалище тампоны или
шарики "Осарцид" (содержат осарсол, борную кислоту, глюкозу по 0,3
гр, стрептоцид 0,5 гр). Применяют также грязевые тампоны из иловой
или торфяной грязи. С целью нормализации влагалищной микрофлоры
назначают промывания растворами с бактериофагами. Завершающим этапом
терапии инфекционно-воспалительных заболеваний мочеполовых органов
независимо от возбудителя, обусловившего патологический процесс,
является коррекция дисбактериоза влагалища.
Назначение тампонов (по 5 доз препарата на тампон) или свечей с
пробиотиками (чередуя): бифидумбактерин, ацилакт или лактобактерин
1-2 раза в день в течение 10-12 суток.
К местному лечению можно
отнести и физиотерапевтические процедуры. Это и диатермия простаты,
и ультразвуковая терапия, ионофорез, фонофорез, лазерная и магнитная
терапия. Их применяют по обычным показаниям.
При выборе антибиотиков
для лечения неспецифических воспалительных заболеваний
урогенитального тракта следует учитывать их негативное действие на
уже сложившийся микробиоценоз организма, особенно при обнаружении у
пациента дисбактериоза кишечника. Поскольку антибактериальная
терапия сопровождается возникновением или усилением кишечных
расстройств, то необходима их коррекция. Сначала нормализуют
деятельность желудочно-кишечного тракта при помощи витаминов группы
В, спазмолитиков, ферментов. Одновременно с этим применяют
бактериофаги (микроорганизмы, "пожирающие" микробную клетку
изнутри), энтеросорбенты (полифенан, полисорб, смекта, энтерогель,
карболен), адаптогены (настойка элеутрококка). Начиная со 2-й недели
от начала лечения кишечник заселяют нормальной микрофлорой при
помощи пробиотиков (колибактерин, бифидумбактерин, лактобактерин,
бификол, ацилакт). Выбор препарата зависит от вида "недостающих"
групп нормальной микрофлоры кишечника.
Критерии излеченности.
При установлении
критериев излеченности трихомониаза необходимо различать
этиологическое и клиническое выздоровление.
Под этиологическим
выздоровлением подразумевается стойкое исчезновение T.vaginalis
из мочеполовых путей пациента после проведённой терапии, которое
подтверждается при микроскопии, культуральным методом и ПЦР.
После окончания лечения
на 7-10 день у мужчин проводят пальпаторное исследование
предстательной железы и семенных пузырьков, производят микроскопию
их секрета. Спустя 12-14 дней после окончания терапии осуществляют
провокацию (алиментарную, местную, медикаментозную или
комбинированную). В том случае, если после провокации в отделяемом
секрете или соскобе со слизистой уретры и в первой порции
свежевыпущенной мочи трихомонады не обнаружены, а также отсутствуют
симптомы уретрита (простатита) - больному рекомендуется через 1
месяц произвести повторное микроскопическое исследование,
уретроскопию и, при необходимости, повторную провокацию.
Первые контрольные
исследования у женщин проводят через 7-8 дней после окончания
антитрихомонадного лечения. В дальнейшем обследование проводится в
течение трёх менструальных циклов. Лабораторный контроль
осуществляется непосредственно перед менструацией или через 1-2 дня
после её окончания. Материал для исследования следует брать из всех
возможных очагов поражения.
Больные считаются
этиологически излеченными, когда после окончания комплексного
лечения при неоднократных повторных обследованиях не удаётся
обнаружить трихомонады в течение 1-2 месяцев у мужчин и 2-3 месяцев
у женщин.
Наиболее часто
посттрихомонадные воспалительные процессы наблюдаются у мужчин с
осложнёнными, хроническими формами трихомониаза. Отсутствие полного
регресса симптомов заболевания при этиологическом излечении
трихомониаза у женщин и мужчин скорее всего свидетельствует о
наличии других инфектов, передаваемых половым путём, или об
активизации условно-патогенной флоры урогенитального тракта,
ассоциированных с трихомонадами.
|

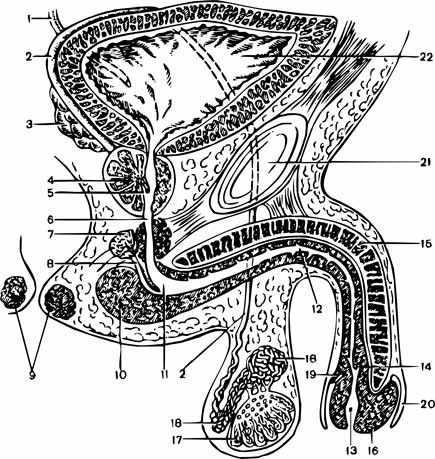

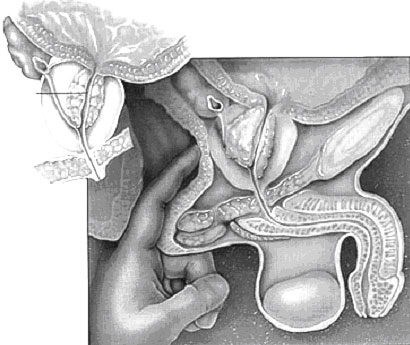











 оболочки
полового члена. Патология сопровождается
образованием фиброзной неэластичной рубцовой
ткани белочной оболочки и прилегающей
кавернозной ткани и приводит к возникновению
болезненных эрекций, искривлению эрегированного
пениса, иногда – к эректильной
дисфункции. Затруднение или невозможность
проведения коитуса (полового акта) при болезни
Пейрони, в свою очередь, приводит к стойкому
нарушению психосексуального состояния мужчины.
оболочки
полового члена. Патология сопровождается
образованием фиброзной неэластичной рубцовой
ткани белочной оболочки и прилегающей
кавернозной ткани и приводит к возникновению
болезненных эрекций, искривлению эрегированного
пениса, иногда – к эректильной
дисфункции. Затруднение или невозможность
проведения коитуса (полового акта) при болезни
Пейрони, в свою очередь, приводит к стойкому
нарушению психосексуального состояния мужчины.
 (наподобие
покрышки автомобиля с накачанной внутри
камерой). Это придает необходимую для проведения
коитуса (полового акта) твердость половому
члену.
(наподобие
покрышки автомобиля с накачанной внутри
камерой). Это придает необходимую для проведения
коитуса (полового акта) твердость половому
члену.